抗击疫情医药行业相关上市公司贡献与影响梳理
疫情检测:以核酸检测试剂盒为主,分子诊断企业获益目前国内已有近百家企业参与了新型冠状病毒检测试剂盒研发的工作,各类检测产品纷纷报证,从目前的公开信息上看,此类产品主要是以核酸检测为主、免疫检测为辅。
核酸检测是目前临床上确诊新型冠状病毒感染的“金标准”,技术方法成熟,灵敏度高。截至目前,已有7种检测产品已获得国家药监局产品注册证。这些产品中以实时荧光RT-PCR检测方法为主,少数是以基因测序进行诊断。
华大基因:公司的两款产品一款是基于宏基因组测序(联合探针锚定聚合测序法)的检测试剂盒,另一款是基于RT-PCR技术的检测试剂盒。结合RT-PCR技术和宏基因组测序两个检测方法,可更快、更全面覆盖2019-nCoV病毒检测,并监测新型冠状病毒在传播过程中可能会发生的变异。从实际使用上看,大多数医院没有测序的设备,且需要生物信息团队来协助测序结果的解读,所以现在的诊断方法以RT-PCR为主。但由于新型冠状病毒在传播过程中可能会发生变异,影响RT-PCR检测的敏感性,所以华大基因在超高通量测序仪上采用高敏PMseq-RNA检测技术,以弥补RT-PCR的缺点,有效提高阳性率,并可监测可能的变异。
之江生物:公司产品是目前已获批产品中唯一可以同时检测三个靶基因的产品,增加一个病毒基因的检测靶点,可能会因此增加检测实验量,造成检测效能降低,但也可能因此而提升检出率,降低“假阴性”。
达安基因和另外3家企业的检测产品,基本“同质化”,均为依托RT-PCR技术检测病毒2处靶基因,但结合公司各自检测平台,检测效能可能有所不同。如圣湘生物结合自主研发的全自动核酸提取仪,单批检测样本量可达96人份,能实现1人1机1日检测样本量达1000人份以上的高通量检测;结合圣湘生物移动分子诊断平台(POCT),最快可在30分钟出检测结果,实现现场即时检测。
表:已获批上市的7种2019-nCoV检测产品
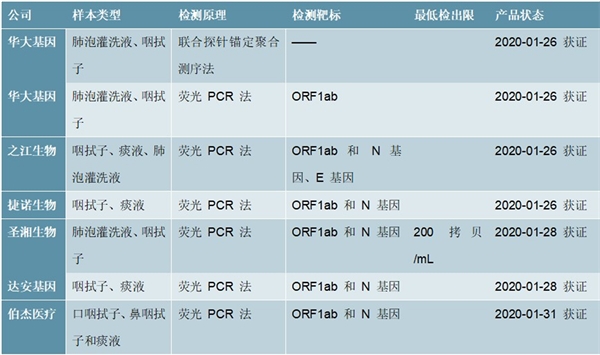
资料来源:资料来源:国家药监局、公司公告、锐观咨询整理
处在注册通道中的产品还有达安基因、硕世生物、凯普生物、万孚生物等推出的分子检测和测序试剂盒。
万孚生物:目前万孚生物研发了三种新冠病毒检测产品,涵盖了核酸、抗原和抗体检测。其中核酸类检测产品有通用型的荧光RT-PCR检测试剂,也有配合万孚检测平台的全自动封闭式核酸检测试剂;而胶体金法检测本身对场景要求和检验人员的熟练程度要求均不高,时效上可在30min内完成检验,但由于机体感染病毒后,不同检测方法的窗口期(从感染至能够被技术检测出的时间)不同,一般将抗原、抗体进行联检效果较好。
凯普生物、贝瑞基因分别推出了基于基因测序技术的诊断产品,加之华大基因的相关测序产品,涵盖了目前第一代(凯普生物)、第二代(华大基因)、第三代(贝瑞基因)基因测序技术。总的来看,一代技术成熟且准确率高,但通量低且成本高,难以进行大规模筛查;二代技术相较一代,通量高且成本低,但技术相对复杂,数据分析需要生物信息学专业人员进行;而三代技术与一代、二代相比,无需PCR提升时效,且通量高成本低,但目前技术相对不成熟,准确率有待提升。
表:三代2019-nCoV测序产品对比

资料来源:资料来源:国家药监局、公司公告、锐观咨询整理
表:暂未上市的各类2019-nCoV检测产品
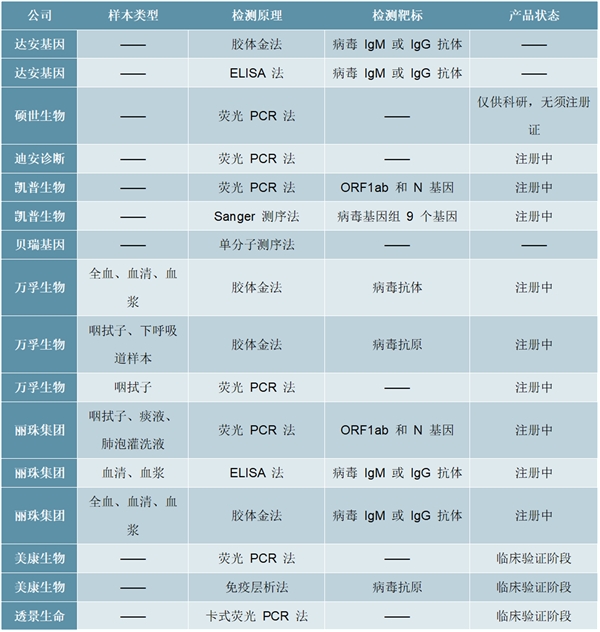
资料来源:资料来源:国家药监局、公司公告、锐观咨询整理
从目前核酸诊断的实际效果看,在感染患者中,阳性率不高,存在着“假阴性”的情况,其原因可能为:
1)检测样品为呼吸道分泌物,且新型冠状病毒主要感染下呼吸道,因此采集部位对检测结果的影响较大,如采样不当,可能产生“假阴性”的结果。目前肺泡、痰液等下呼吸道样本的检测准确率最高,但采集过程需要局部麻醉后将纤维支气管镜插入右肺中叶或左肺舌段的支管,经气管活检孔加入无菌生理盐水,得到灌洗液,采集难度大且操作者容易感染;而鼻咽拭子采样来自口腔黏膜或鼻腔,采样相对方便,但距离下呼吸道感染部位较远,不是最佳的采样部位。
2)患者的病程与病情不同,在相关部位采集不到病毒或采集到的病毒量太少,也可能产生“假阴性”结果,需要病毒达到一定浓度才能检测到,如果拷贝数低于下限则会检测不出来或者数据不稳定,产生“假阴性”,以圣湘生物的新冠病毒的核酸检测试剂为例,其最低检出限为200拷贝/mL。
3)标本运输及保存过程中,由于2019-nCoV为RNA病毒,容易被外源性或细胞破坏后所释放的RNA酶降解,而影响最后的检测效率,一般建议采样后4h内进行检测,如不能及时检测,一般可置于4℃保存24h或-70℃冻存,但长期保存或反复冻融可能对样品质量产生影响。
4)在核酸提取环节中,实验室采用手工提取或机器全自动/半自动提取,不同的提取流程使得核酸提取产物的数量和质量有差异,将直接影响最后的检测结果。
5)在核酸扩增环节中,不同厂家试剂中酶、金属离子等成分与质量的差异,可能影响扩增效率和最后检测结果的灵敏度。
6)不同实验室用于2019-nCoV核酸检测的仪器种类有所不同,价格上从几万、十几万、数十上百万不等,不同的设备对检测过程中不同温度的控制精度、对荧光信号检测敏感度等不同,从而可能导致检测结果的差异。
7)除了技术方法理论上和疾病本身因素产生“假阴性”结果的原因外,试剂盒的质量也是不容忽视的一个要素。由于此次疫情紧急,许多试剂盒在早期研发的时候,可能没有足够时间如正常流程完成试剂的优化和质控、灵敏度和特异性测试等,因此导致灵敏度不够,检测的结果不稳定。正常情况下IVD三类诊断试剂盒从研发到临床再到拿证需要3-5年,甚至更久。期间需历经临床预实验来验证试剂盒是否有效,和正式的临床试验来验证试剂盒的灵敏度和特异性是否符合预期,在相关临床试验通过并质检合格后,才能进行注册审批,进行正式生产和投入临床使用。
免疫检测产品目前尚未有产品获得医疗器械注册证,相关检测方法尚未列入《新型冠状病毒肺炎诊疗方案》中。目前已有少量公司宣布成功研发出新型冠状病毒免疫检测产品,主要是依赖ELISA法和胶体金法,可分别检测病毒抗原和/或抗体,相关产品正处在临床验证或注册审批阶段。由于免疫类检测产品在感染伊始,可能由于机体尚未产生抗体或抗原量少,无法获得阳性结果,因此可作为核酸检测的辅助手段,排除核酸检测中可能出现的“假阳性”或“假阴性”;除此以外,胶体金免疫层析法因其检测时效高、对检测环境和操作人员要求低,可以作为机场、车站、公路、大型公共场所现场初筛使用。
2月8日,科技部发布《新型冠状病毒(2019-nCoV)现场快速检测产品研发应急项目申报指南的通知》,该指南旨在面向社会广泛征集新型冠状病毒的现场快速检测产品,突破现有检测技术对人员/场所的限制,缩短检测用时,提升便捷程度,推动诊断前移下移,实现疑似患者的快速诊断和密切接触人群的现场筛查。针对核酸、抗原、抗体的三大类快速检测试剂,该指南分别提出了具体要求:
表:POCT类检测产品要求
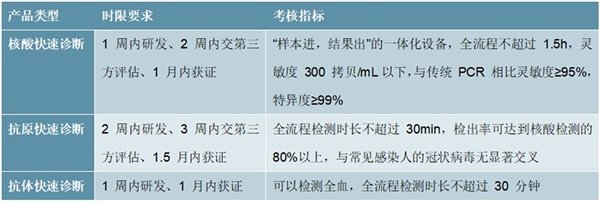
资料来源:公开资料整理