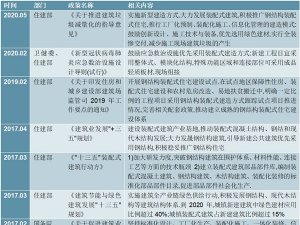
化学药品原料药制行业监管体制及主要政策
1、化学药品原料药制行业主管部门
医药行业的主管部门是国家卫生和计划生育委员会、国家发展和改革委员会以及国家各级食品药品监督管理部门。
国家卫生和计划生育委员会主要负责推进医药卫生体制改革、负责建立国家基本药物制度并组织实施、统筹规划与协调全国卫生资源配置。
国家发展和改革委员会负责研究拟定医药行业发展规划,推进落实医药工业产业政策,指导行业结构调整以及实施行业管理;制订药品价格政策,监督价格政策的执行,调控药品价格总水平。
国家食品药品监督管理总局为国务院直属机构,主管全国药品监督管理工作,主要负责起草药品监督管理的法律法规草案,拟订政策规划,制定部门规章;负责组织制定、公布国家药典等药品标准、分类管理制度并监督实施;负责制定药品研制、生产、经营、使用质量管理规范并监督实施;负责药品注册并监督检查;负责指导地方食品药品监督管理工作。省、自治区、直辖市食品药品监督管理部门负责本行政区域内的药品监督管理工作。
2、化学药品原料药制行业管理体制
医药企业必须遵循医药行业管理体制,该体制主要围绕三个方面:药品生产经营行业准入许可、强制性质量管理规范认证、药品注册管理。具体包括:药品生产许可证制度、药品生产质量管理规范(GMP)、药品注册管理制度、国家药品标准制度、药品价格管理制度、处方药和非处方药分类管理制度等。医药行业管理体制依据《中华人民共和国药品管理法》及实施条例,以及各细分管理办法、规范及标准执行。
(1)药品生产许可制度
根据《中华人民共和国药品管理法》(主席令第45号)第七条规定,开办药品生产企业,须经企业所在地省、自治区、直辖市人民政府药品监督管理部门批准并发给《药品生产许可证》。无《药品生产许可证》的,不得生产药品。《药品生产许可证》应当标明有效期和生产范围,到期重新审查发证。
(2)药品生产质量管理规范制度
根据《中华人民共和国药品管理法》(主席令第45号)第九条规定,药品生产企业必须按照国务院药品监督管理部门依据本法制定的《药品生产质量管理规范》组织生产。药品监督管理部门按照规定对药品生产企业是否符合《药品生产质量管理规范》的要求进行认证;对认证合格的,发给认证证书。
(3)药品注册管理制度
根据《药品注册管理办法》(局令第28号),药品注册管理制度包括新药申请、新药监测期、仿制药申请和再注册申请等。
①新药申请
新药申请,是指未曾在中国境内上市销售的药品的注册申请。对已上市药品改变剂型、改变给药途径、增加新适应症的药品注册按照新药申请的程序申报。
改变剂型但不改变给药途径,以及增加新适应症的注册申请获得批准后不发给新药证书;靶向制剂、缓释、控释制剂等特殊剂型除外。
②新药监测期
国家食药监局根据保护公众健康的要求,可以对批准生产的新药品种设立监测期。监测期自新药批准生产之日起计算,最长不得超过5年。监测期内的新药,国家食药监局不批准其他企业生产、改变剂型和进口。新药进入监测期之日起,国家食药监局已经批准其他申请人进行药物临床试验的,可以按照药品注册申报与审批程序继续办理该申请,符合规定的,国家食药监局批准该新药的生产或者进口,并对境内药品生产企业生产的该新药一并进行监测。
新药进入监测期之日起,不再受理其他申请人的同品种注册申请。已经受理但尚未批准进行药物临床试验的其他申请人同品种申请予以退回;新药监测期满后,申请人可以提出仿制药申请或者进口药品申请。
③仿制药申请
仿制药申请,是指生产国家食药监局已批准上市的已有国家标准的药品的注册申请;但是生物制品按照新药申请的程序申报。仿制药申请人应当是药品生产企业,其申请的药品应当与《药品生产许可证》载明的生产范围一致。
④再注册申请
再注册申请,是指药品批准证明文件有效期满后申请人拟继续生产或者进口该药品的注册申请。国家食药监局核发的药品批准文号、《进口药品注册证》或者《医药产品注册证》的有效期为5年。有效期届满,需要继续生产或者进口的,申请人应当在有效期届满前6个月申请再注册。
(4)国家药品标准制度
国家药品标准是指国家为保证药品质量所制定的质量指标、检验方法以及生产工艺等的技术要求,包括《中华人民共和国药典》、《中华人民共和国卫生部药品标准》、《国家食品药品监督管理局国家药品标准》等。国务院药品监督管理部门组织药典委员会负责国家药品标准的制定和修订。国家药品标准没有规定的,须按照省、自治区、直辖市人民政府食品药品监督管理部门制定的规范标准执行。
(5)国家基本药物制度
2009年3月17日国务院发布的《关于深化医药卫生体制改革的意见》指出,我国将建立国家基本药物制度。中央政府统一制定和发布国家基本药物目录。
2009年8月18日,国家发改委、卫生部等9部委发布了《关于建立国家基本药物制度的实施意见》,标志着我国建立国家基本药物制度工作正式实施。2013年3月13日,卫生部发布了《国家基本药物目录(2012版)》,该目录分为化学药品和生物制品、中成药、中药饮片三个部分,其中,化学药品和生物制品317种,中成药203种,中药饮片不列具体品种,共计520种。
(6)药品价格管理制度
根据《中华人民共和国药品管理法》第五十五条规定,依法实行市场调节价的药品,药品的生产企业、经营企业和医疗机构应当按照公平、合理和诚实信用、质价相符的原则制定价格,为用药者提供价格合理的药品。药品的生产企业、经营企业和医疗机构应当遵守国务院价格主管部门关于药价管理的规定,制定和标明药品零售价格,禁止暴利和损害用药者利益的价格欺诈行为。
2015年5月4日,国家发展改革委会同国家卫生计生委、人力资源和社会保障部等部门联合发出《关于印发推进药品价格改革意见的通知》(发改价格[2015]904号),决定从2015年6月1日起取消除麻醉药品和第一类精神药品外药品政府定价,完善药品采购机制,发挥医保控费作用,药品实际交易价格主要由市场竞争形成。此前有关药品价格管理政策规定,凡与该通知规定不符的一律废止,以该通知规定为准。
该通知附件《推进药品价格改革的意见》对改革药品价格形成机制进行了具体规定:(一)医保基金支付的药品,由医保部门会同有关部门拟定医保药品支付标准制定的程序、依据、方法等规则,探索建立引导药品价格合理形成的机制;(二)专利药品、独家生产药品,建立公开透明、多方参与的谈判机制形成价格;„„(四)麻醉药品和第一类精神药品,仍暂时实行最高出厂价格和最高零售价格管理;(五)其他药品,由生产经营者依据生产经营成本和市场供求情况,自主制定价格。
(7)处方药和非处方药分类管理制度
我国实行处方药和非处方药分类管理制度。根据《处方药与非处方药分类管理办法(试行)》(局令第10号)规定,根据药品品种、规格、适应症、剂量及给药途径不同,对药品分别按处方药与非处方药进行管理。处方药必须凭执业医师或执业助理医师处方才可调配、购买和使用;非处方药不需要凭执业医师或执业助理医师处方即可自行判断、购买和使用。国家药品监督管理局负责处方药与非处方药分类管理办法的制定。各级药品监督管理部门负责辖区内处方药与非处方药分类管理的组织实施和监督管理。
3、化学药品原料药制行业主要法律、法规及适用标准
医药行业的主要法律、法规及适用标准如下表所示:
2001-02-28、2001-12-01、全国人民代表大会常务委员会、《中华人民共和国药品管理法》、主席令第45号
2002-08-04、2002-09-15、国务院、《中华人民共和国药品管理法实施条例》、国务院令第360号
2007-07-10、2007-10-01、国家食药监局、《药品注册管理办法》药品生产质量管理规范(2010年修i)、局令第28号
2011-01-17、2011-03-01、卫生部、《药品不良反应报告和监测管理办法》、卫生部令第79号
2011-05-04、2011-07-01、卫生部、《药品召回管理办法》、卫生部令第81号
2007-12-10、2007-12-10、国家食药监局、《药品说明书和标签管理规定》、局令第29号
2006-03-15、2006-06-01、国家食药监局、《药品生产监督管理办法》、局令第24号
2004-08-05、2004-08-05、国家食药监局、《直接接触药品的包装材料和容器管理办法》、局令第14号
2004-07-20、2004-07-20、国家食药监局、《药品包装用材料、容器管理办法》(暂行)、局令第13号
2000-04-29、2000-10-01、国家食药监局、处方药与非处方药分类管理办法(试行)、局令第21号
1999-06-18、2000-01-01、国家食药监局、处方药与非处方药分类管理办法(试行)、局令第10号
2009-07-31、国家食药监局、《关于做好药品再注册审查审批工作的通知》、国食药监注(2009)387号
2010-09-29、国家食药监局、《关于做好药品再注册审查审批工作的补充通知》、国食药监注(2010)394号
2015-06-05、2015-12-01、国家食药监局、《中华人民共和国药典》2015年版、国家食药监局公告2015年第67号
2016-03-04、2016-03-04、国家食药监局、《总局关于发布化学药品注册分类改革工作方案的公告》、2016年第51号
2016-05-26、2016-05-26、国务院办公厅、《国务院办公厅关于印发、国办发(2016)41号
2016-04-21、国务院办公厅、药品上市许可持有人制度、国办发(2016)26号
(二)化学药品原料药制行业相关发展规划及政策:
1、国民经济和社会发展第十三个五年规划纲要
国民经济和社会发展第十三个五年规划纲要第六章《强化科技创新引领作用》第一节“推动战略前沿领域创新突破”中指出:坚持战略和前沿导向,集中支持事关发展全局的基础研究和共性关键技术研究,更加重视原始创新和颠覆性技术创新。聚焦目标、突出重点,加快实施已有国家重大科技专项,部署启动一批新的重大科技项目。加快突破新一代信息通信、新能源、新材料、航空航天、生物医药、智能制造等领域核心技术。加强深海、深地、深空、深蓝等领域的战略高技术部署......。
国民经济和社会发展第十三个五年规划纲要第四十一章《拓展蓝色经济空间》第一节“壮大海洋经济”中指出:优化海洋产业结构,发展远洋渔业,推动海水淡化规模化应用,扶持海洋生物医药、海洋装备制造等产业发展,加快发展海洋服务业。发展海洋科学技术,重点在深水、绿色、安全的海洋高技术领域取得突破。推进智慧海洋工程建设。创新海域海岛资源市场化配置方式。深入推进山东、浙江、广东、福建、天津等全国海洋经济发展试点区建设......。
2、《国务院关于加快培育和发展战略性新兴产业的决定》
国发[2010]32号文中指出要努力实现重点领域快速健康发展,其中包括生物产业。并提出要大力发展用于重大疾病防治的生物技术药物、新型疫苗和诊断试剂、化学药物、现代中药等创新药物大品种,提升生物医药产业水平……推进生物制造关键技术开发、示范与应用。加快海洋生物技术及产品的研发和产业化。
3、《医药工业发展规划指南》(工信部联规[2016]350号)
工业和信息化部、国家发展和改革委员会、科学技术部、商务部等六部委2016年10月联合印发的《医药工业发展规划指南》中指出:医药工业是关系国计民生的重要产业,是中国制造2025和战略性新兴产业的重点领域,是推进健康中国建设的重要保障。把握产业技术进步方向,瞄准市场重大需求,大力发展生物药、化学药新品种、优质中药等,加快各领域新技术的开发和应用,促进产品、技术、质量升级。……优化出口结构,促进出口增长。巩固化学原料药国际竞争地位,提高精深加工产品出口比重,增加符合先进水平GMP要求的品种数量。立足原料药产业优势,实施制剂国际化战略,全面提高我国制剂出口规模、比重和产品附加值,重点拓展发达国家市场和新兴医药市场。
《医药工业发展规划指南》还指出,培育支持中小企业上市,促使企业规范公司治理结构,转换经营机制。鼓励社会资本发展并购基金,拓宽企业兼并重组融资渠道。
4、《国务院关于印发生物产业发展规划的通知》(国发[2012]65号)
国务院2012年12月发布的《国务院关于印发生物产业发展规划的通知》指出要突出高品质发展,提升生物医药产业竞争力。以满足不断增长的健康需求和增强产业竞争力为目标,组织实施生物技术药物发展等行动计划,通过完善新药研制基础支撑平台和共性技术平台、开展产业化示范应用、加强先进技术规范推广应用和完善医药管理体制机制等,全面提升生物医药企业的创新能力和产品质量管理能力,加快生物技术药物、化学药物、中药等新产品与新工艺开发和产业化,增强区域支撑配套能力,积极推动行业结构调整,做大做强生物医药产业。
该发展规划中还提到要加强海洋生物资源开发利用。其中指出加快海洋生物活性物质的开发应用,发展工业用酶、医用功能材料、生物分离材料、绿色农用生物制剂、创新药物等海洋新产品。建设海洋生物库等产业发展公共服务平台。
提高海洋水产综合加工技术及加工废弃物高值化利用水平,加强远洋生物资源探捕开发,提高远洋新品种的利用水平。
5、《国务院办公厅关于促进医药产业健康发展的指导意见》(国办发[2016]11号)
国务院办公厅2016年3月4日发布的《国务院办公厅关于促进医药产业健康发展的指导意见》指出,医药产业是支撑发展医疗卫生事业和健康服务业的重要基础,是具有较强成长性、关联性和带动性的朝阳产业,在惠民生、稳增长方面发挥了积极作用。