CMOCDMO行业监管体制及主要政策
1、CMOCDMO行业主管部门和监管体制
(1)CRO行业的监管
CRO行业主要为药企及科研单位提供从新药的发现、研发到开发的一体化服务,伴随新药研发的全流程,因其服务领域的专业性和特殊性而与医药行业的发展紧密相关。我国对药品的研发、研究、生产、流通和使用进行全过程监督管理的机构为国家食药监局,各省、自治区和直辖市人民政府食品药品监督管理部门负责本行政区域内的药品相关日常监督管理工作。
2003年,CFDA制定了《药物非临床研究质量管理规范》(国家食品药品监督管理局令第2号)及《药物临床试验质量管理规范》(国家食品药品监督管理局令第3号),规范了国内药物的非临床研究和临床工作。发行人作为从事医药研发专业服务机构直接参与药物研究的全产业链工作,其执业过程亦需受CFDA管理,并受到各级政府食品药品监督管理部门的日常监督管理。此外,由于发行人主营业务中涉及的临床前CRO业务中部分实验主要通过动物实验进行,适用中华人民共和国科学技术部颁布的《实验动物管理条例》(2017年修
订)(国家科学技术委员会令第2号)的管辖,因此发行人亦受我国科技部的管理及各级地方科技行政部门的日常监督管理。
由于发行人的主要客户为大型跨国药企,为全球客户提供新药研发支持服务,以美国、欧洲市场为主,故其在上述地区的主营业务会分别受到国际人用药品注册技术协调会(ICH)、美国食品药品监督管理局(FDA)、欧洲药品管理局(EMA)及欧洲药品质量管理局(EDQM)的监管并需遵守各自所在地的日常监督管理规范。过往FDA及EMA曾制定了详细的GLP、GCP和GMP等各项药品非临床、临床及生产质量管理规范,FDA近期也发布了《IND申办人与FDA沟通规范新版指南草案》等文件,对非临床研究要求、临床设计以及药品生产等医药行业全产业链日常业务运营形成详细的监管要求。
2017年6月19日,国家食药监局与国际人用药品注册技术协调会(ICH)同时宣布,ICH正式批准国家食药监局成为其成员。加入ICH,意味着中国药品监管部门、制药行业和研发机构,将逐步转化和实施国际最高技术标准和指南,并参与规则制定,推动国际创新药品早日进入中国市场,有效提升国内制药产业创新能力和国际竞争力。
(2)CMO/CDMO行业的监管:
由于CMO/CDMO业务的日常业务主要为接受药企委托,其进行药品工艺开发、配方开发以及临床用药、中间体制造、原料药生产、制剂生产、包装等定制生产制造服务,因此CMO/CDMO行业亦受到CFDA及下属各级食品药品监督管理部门的监督管理。
此外,发行人在向跨国制药公司提供CMO/CDMO业务时,交付的最终产品有相当一部分是以原料药起始物料、cGMP中间体或其他形式进行提供。由于医药中间体属于精细化学品,而国家发改委及其各级下属机构负责精细化工行业政策的研究制定、产品开发、推广指导、项目审批等监督及管理,故发行人仍需受到国家发改委及下属各级发改部门的日常监督管理。
2、主要法律法规、政策:
(1)医药行业主要政策:
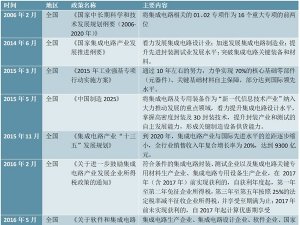
2010年10月10日国务院关于加快培育和发展战略性新兴产业的决定明确将生物医药产业纳入我国战略性新兴产业范畴,要求大力发展用于重大疾病防治的生物技术药物、新型疫苗和诊断试剂、化学药物、现代中药等创新药物大品种,提升生物医药产业水平。加快先进医疗设备、医用材料等生物医学工程产品的研发和产业化。
2010年10月9日关于加快医药行业结构调整的指导意见鼓励医药企业技术创新,加大对医药研发的投入,鼓励开展基础性研究和开发共性、关键性以及前沿性重大医药研发课题。支持企业加强技术中心建设,通过产学研整合技术资源,推动企业成为技术创新的主体。
2016年3月16日中华人民共和国国民经济和社会发展第十三个五年规划纲要十三五规划纲要对医药产业在今后五年的发展做出了重要规划。其中,规划提出“鼓励研究和创制新药,将已上市创新药和通过一致性评价的药品优先列入医保目录”。
2016年12月27日“十三五”深化医药卫生体制改革规划“十三五”期间,要在分级诊疗、现代医院管理、全民医保、药品供应保障、综合监管等5项制度建设上取得新突破,同时统筹推进相关领域改革。
2016年12月28日《全国药品流通行业发展规划纲要(2016-2020)》提出合理规划行业布局、健全药品流通网络,提升流通管理水平、打造现代医药供应商,创新行业经营模式、拓展行业服务功能,“引进来”与“走出去”商务部相结合、提升行业开放水平,加强行业基础建设、提高行业服务能力等五项主要任务。
2016年10月26日医药工业发展规划指南推进生物药、化学药新品种、优质中药、高性能医疗器械、新型辅料包材和制药设备六大重点领域发展,加快各领域新技术的开发和应用,促进产品、技术、质量升级。推进化学仿制药质量升级计划、中药材资源可持续利用计划、中药质量提升计划、疫苗质量提升计划、医疗器械质量提升计划,促进质量安全水平提升和产业升级。
2018年1月30日关于加强和促进食品药品科技创新工作的指导意见以相关国家科技计划(专项、基金等)为依托,加大对群众急需的重点药品、创新药、先进医疗器械自主创新等支持力度。发挥企业技术创新的主体作用,以监管法规政策和相关科技计划(专项、基金)为依托,引领食品药品企业在新产品研发、工艺创新和已上市产品再评价等方面加强研究。鼓励采用新技术、新设备、新材料,对现有设施、工艺条件及生产服务等进行改造提升,指导和帮助企业提高自我检测和评价能力,增强创新和竞争能力。推进食品药品标准基础研究,充分发挥标准对企业研发的引领作用。
(2)我国的CRO/CMO/CDMO行业监管政策
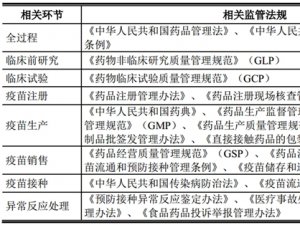
围绕提高药品安全性、有效性和质量可控性,我国建立了涵盖药品研究、生产、流通、使用各环节的监管制度,公司所属医药研发服务行业适用的主要法律法规、规范性文件及基本情况如下:
2015年4月24日研制新药,必须按照国务院药品监督管理部门的规定如实报送研制方法、质量指标、药理及毒理结果等有关资料和样品,经国务院药品监督管理部门批准后,方可进行临床。药物的非临床安全性评价研究机构和临床机构必须分别执行药物非临床研究质量管理规范、药物临床质量管理规范。
2016年2月6日药物临床申请经国务院药品监督管理部门批准后,申报人应当在经依法认定的具有药物临床资格的机构中选择承担药物临床的机构。药物临床机构进行药物临床,应当事先告知受试者或者其监护人真实情况,并取得其书面同意。
2007年10月1日规定了新药申请、仿制药申请、进口药品申请及其补充申请和再注册申请的管理办法,包括药物注册的基本要求、临床、新药申请、仿制药及进口药的申报与审批、非处方药的申报、药品再注册、药品注册检验等,其中规定了药物申请所需进行的各期临床内容与要求,明确了临床中需审核和备案的关键程序,以及临床中不良事件的应对措施等。
2012年8月24日规定了进口药品的备案、报关、口岸检验等程序,包括了进口单位向允许药品进口的口岸所在地药品监督管理部门申办《进口药品通关单》,以及药品检验机构对抵达口岸的进口药品依法实施检验工作的过程。
2005年11月18日规定了突发公共卫生事件中应急所需防治药品的特别审批程序,以及该审批程序中对于应急药品进行临床的相关流程及要求。
2009年1月7日规定了符合国家食药监局设定的创新药条件的新药注册申请的特殊审批办法,包括注册申请的材料、申请流程、临床要求等。
2003年9月1日参照国际公认准则,规定了临床标准全过程,包括前的准备及必要条件、受试者的权益保障、研究者、申办者及监察员的职责、方案设计、组织实施、监察、稽查、记录与报告、数据管理与统计分析、用药品管理、质量保证和多中心。
2010年11月2日参照国际公认准则,规定了药物临床的伦理审查工作,包括伦理委员会的组织与管理、职责要求,伦理审查的申请与受理,伦理委员会的伦理审查,伦理审查的决定与送达,以及伦理审查后的跟踪审查等。
2011年12月2日规范了药物临床中生物样本分析实验室的管理工作,包括组织结构和人员、实验室设施、仪器与材料、合同管理、标准操作规程和实验的实施,以及生物样本分析数据的质量和管理等。
2011年12月2日参照国际标准,规范指导了药物I期临床的组织管理与实施,包括职责要求、实施条件、质量保证、风险管理、合同和协议、方案、受试者管理、用药品管理、生物样本管理和分析、数据管理和统计分析,以及总结报告等。
2015年8月9日就如何提高审评审批质量、解决注册申请积压、提高仿制药质量、鼓励研究和创制新药、提高审评审批透明度等目标提出改革方向和措施。
2015年11月11日为解决药品注册申请积压问题,提高药品审评审批质量和效率,CFDA提出实行若干药品注册审评审批新政策。
2016年2月6日通过仿制药质量一致性评价,初步建立仿制药参比制剂目录,逐步完善仿制药质量评价体系,淘汰内在质量和临床疗效达不到要求的品种,促进我国仿制药整体水平提升。
2016年5月26日体现了药品注册管理制度向上市许可持有人制度转变的核心理念,即鼓励新药创制,促进产业升级,优化资源配置,落实主体责任。
2017年1月24日体现了提高药品质量疗效,整顿药品流通秩序,规范医疗和用药行为,推进健康中国建设。
2017年5月11日临床试验机构资格认定改为备案管理,支持研究者和临床试验机构开展临床试验,完善伦理委员会机制,提高伦理审查效率,优化临床试验审查程序,接受境外临床试验数据,支持拓展性临床试验。
2017年10月8日推进医药产业转入创新驱动发展轨道,坚持鼓励新药创新医疗器械研发和提升仿制药质量疗效。
(3)精细化工行业监管政策
发行人日常CMO/CDMO业务多集中于精细化工领域的研发与制造。作为CMO/CDMO企业,其生产活动受到《中华人民共和国环境保护法》(2014年修订)、《中华人民共和国安全生产法》(2014年修订)、《中华人民共和国产品质量法》(2009年修订)等法律法规的约束。发行人应当遵守的行业主要法律法规包括:
实施日期名称相关内容
2015年1月1日中华人民共和国环境保护法(2014年修订)为保护和改善环境,防治污染和其他公害,保障公众健康,推进生态文明建设,促进经济社会可持续发展制定的国家法律。
1997年3月1日中华人民共和国环境噪声污染防治法为防治环境噪声污染,保护和改善生活环境,保障人体健康,促进经济和社会发展制定。
2016年1月1日中华人民共和国大气污染防治法(2015年修订) 为保护和改善环境,防治大气污染,保障公众健康,推进生态文明建设,促进经济社会可持续发展制定。
2012年7月1日中华人民共和国清洁生产促进法(2012年修订) 为促进清洁生产,提高资源利用效率,减少和避免污染物的产生,保护和改善环境,保障人体健康,促进经济与社会可持续发展制定。
2016年7月2日中华人民共和国环境影响评价法(2016年修订) 为了实施可持续发展战略,预防因规划和建设项目实施后对环境造成不良影响,促进经济、社会和环境的协调发展,制定本法。
2016年11月7日中华人民共和国固体废物污染环境防治法(2016年修订) 为了防治固体废物污染环境,保障人体健康,维护生态安全,促进经济社会可持续发展制定。
2014年12月1日中华人民共和国安全生产法(2014年修订)为了加强安全生产工作,防止和减少生产安全事故,保障人民群众生命和财产安全,促进经济社会持续健康发展制定。
2014年7月29日安全生产许可证条例(2014年修订)为了严格规范安全生产条件,进一步加强安全生产监督管理,防止和减少生产安全事故,根据《中华人民共和国安全生产法》的有关规定制定。
2013年12月7日危险化学品安全管理条例(2013年修订)为了加强危险化学品的安全管理,预防和减少危险化学品事故,保障人民群众生命财产安全,保护环境制定。
2012年8月1日危险化学品登记管理办法为了加强对危险化学品的安全管理,规范危险化学品登记工作,为危险化学品事故预防和应急救援提供技术、信息支持,根据《危险化学品安全管理条例》制定。
2015年5月1日职业健康检查管理办法为了加强职业健康检查工作,规范执业健康检查机构管理,保护劳动者健康制定。
2009年8月27日中华人民共和国产品质量法(2009年修订)为了加强对产品质量的监督管理,提高产品质量水平,明确产品质量责任,保护消费者的合法权益,维护社会经济秩序制定。