创新药行业发展有利因素及不利因素
1、影响行业发展的有利因素:
(1)我国药政改革加速,全方位鼓励创新药发展
2015年可以称作是我国创新药行业的发展元年。对于整个医药行业而言,受招标限价和医保控费等严厉政策的影响,行业增速已下降到10%以下,药品集中审批、新一轮非基药招标、医保对辅助用药的监管强化等一系列药品政策的变化,导致药企传统盈利模式受到挑战,盈利能力持续承压。与此同时,仿制药一致性评价、化学药注册分类改革、创新药优先审评、医保目录动态调整、海外临床试验数据认证、上市许可人制度试点等一系列重磅政策接踵而至,创新药行业面临历史性的发展机遇。
2015年以来鼓励创新药品政策法规出台情况:
出台时间、部门、政策法规
2015年7月、CFDA、征求加快解决药品注册申请积压问题的若干政策意见公告
2015年8月、国务院、关于改革药品医疗器械审评审批制度的意见
2016年2月、CFDA、关于解决药品注册申请积压实行优先审评审批的意见
2016年3月、CFDA、化学药品注册分类改革工作方案
2016年3月、国务院、关于开展仿制药质量和疗效一致性评价的意见
2016年6月、国务院、药品上市许可持有人制度试点方案
2017年4月、人社部、关于公开征求建立完善基本医疗保险、工伤保险和生育保险药品
目录动态调整机制有关意见建议的通知
2017年5月、CFDA、关于鼓励药品医疗器械创新加快新药医疗器械上市审评审批的
相关政策(征求意见稿)
2017年5月、CFDA、关于鼓励药品医疗器械创新改革临床试验管理的相关政策(征求
意见稿)
2017年8月、CFDA、关于推进药品上市许可持有人制度试点工作有关事项的通知
2017年10月、国务院、《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》
2017年10月、CFDA、《<中华人民共和国药品管理法>修正案(草案征求意见稿)》
(2)创新药审评审批进度加速
我国自2015年陆续出台《关于征求加快解决药品注册申请积压问题的若干政策意见的公告》、《国务院关于改革药品医疗器械审评审批制度的意见》、《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》等多项政策,针对国内创新药研发端激励不足、临床试验产能受限、临床和上市申报审批时间过长等多方面困境,为创新药审批上市提速提供了诸多实际利好:
对新药的临床试验申请,实行一次性批准,不再采取分期申报、分期审评审批的方式。
对于具有临床价值的新药和临床急需仿制药进行优先审评审批,明确优先审评范围和审评程序,对新药临床试验申请和生产注册申请的各环节时间进行明确规定。
申请人在欧盟、美国同步申请并获准开展临床试验申请将加快申请,并支持境外多中心取得的临床数据。
取消临床试验机构GLP资质认证,实施备案制,临床试验条件和能力评价纳入医疗机构等级评审,提高临床试验供给、临床试验工作激励制度加强,解锁了临床试验阶段的制约环节。
将药物临床试验审批由明示许可改为默示许可,自受理新药临床试验申请之日起六十个工作日内无异议视为审批通过;并开展药品专利期补偿制度试点。从优先审评的变革结果来看,优先审评品种的上市申请相对非优先审评品种平均加速约33个月,已发批件的优先审评品种所需审批时长亦迅速缩短。
(3)支持创新药逐步纳入医保支付范围
国家政策目前明确鼓励医疗机构优先采购和使用新药。研究完善医疗保险药品目录动态调整机制,改变以往国家医保目录多年保持不变情形,加快支持创新药进入医保目录。探索建立医疗保险药品支付标准国家谈判制度,2017年26个品种通过国家谈判进入国家医保目录。创新药被纳入国家医保目录,保证患者对创新药的支付能力,对创新药的市场销售产生重大影响。此外,国家一类新药在省级招标程序中享有竞争优势,创新药经常在法定招标程序享有优惠待遇,根据
现行的招标政策,由于创新药的质量及功效,其在招标过程中通常被分类为高于仿制药的质量层次。同时,专利创新药在医院采购过程中比仿制药更具优势。
(4)鼓励药物创新,实行上市许可持有人制度
长期以来,我国实行药品注册与生产许可“捆绑”的管理模式,药物研发机构无法成为药品批准文号的持有人,导致我国药品研发创新机制不活、动力不足。
自2015年,全国人民代表大会出台《全国人大常委会关于授权国务院在部分地方开展药品上市许可持有人制度试点和有关问题的决定》,授权国务院组织试点,鼓励药物研发机构或者科研人员等非生产企业主体,可以药品上市许可持有人的身份享有技术创新带来的市场收益。此后,国务院、国家食药总局下发《国务院办公厅关于印发药品上市许可持有人制度试点方案的通知》、《国家食品药品监督管理总局关于推进药品上市许可持有人制度试点工作有关事项的通知》等政策逐步落实开展药品上市许可持有人制度试点工作。这一制度安排必将有效鼓励药物研发机构、科研人员研发药物的主动性、积极性和创造性,激发更多的研发机构和科研人员从事新药创,加快我国新药研发进程。
(5)国家及地方对创新药财政及审批支持加大
“重大新药创制专项”的目标是实现中国药物研究和开发从仿制药的生产向自主创新药物开发的战略转型。国家科技部在每个五年计划实施周期,均组织实施“重大新药科技创制重大专项”,对技术水平领先的新药创制予以资金支持。
同时,各级地方政府也在国家政策号召下,组织各地重大专项评选,对优质项目不断加大财政支持力度。此外,从“重大新药创制专项”输出的创新药物可优先列入国家食药总局的优先审评药物品种,从而得到快速审批。
(6)对仿制药、辅助用药等严格监管,使得创新药市场地位不断提升
2016年2月6日,国务院办公厅发布了《关于开展仿制药质量和疗效一致性评价的意见》(国办发[2016]8号),仿制药一致性评价工作拉开序幕,仿制药的研发难度和研发投入大幅提高,对仿制药企业的盈利能力产生重大影响。
同时,国务院、国家卫计委不断出台政策,加强对辅助用药的监管,不断降低辅助用药临床使用,控制医保费用不合理增长,对于无明确疗效的辅助用药市场需求下降。
受上述影响,创新药在医药行业的市场地位不断提升。
(7)创新药市场未来快速发展
美国是全球最大的医药市场,按销售额计算,其创新的专利药主导市场,2016年占比约为60%。参考美国药品市场格局,在我国药政改革鼓励创新政策的驱动下,IMS预计创新药2021年有望攫取15%份额,而2026年市场份额有望随着企业自身研发能力的进一步强化上升至30%,实现近万亿市场规模。
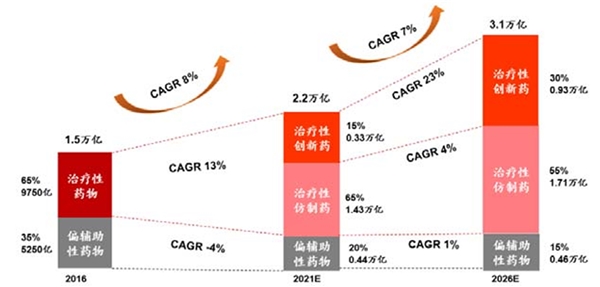
资料来源:公开资料整理
(8)国民收入水平的不断提升,医疗保障体系逐步完善促进医药产业的快速发展
近年来我国居民收入水平不断提升,为我国医疗健康产业的发展奠定了基础。国家统计局发布数据显示,全国城镇居民人均可支配收入从2009年的17,175元增长至2016年的33,616元,年复合增长率为10.07%;全国农村居民人均可
支配收入从2009年的5,153元增长至2016年的12,363元,年复合增长率为13.32%。
2009年以来,我国政府推出的新医改方案,着重于逐步扩大医疗保险覆盖面并提高医疗保险的报销比率,提升中国的整体医疗负担能力、供应能力和药品品质。“十二五”期间,我国继续建设并完善覆盖城乡居民的医疗保障体系,扩大基本医疗保险覆盖面。
随着我国医疗保障体系的不断完善,基本药物目录制度和医保目录的推行,社区和农村医疗卫生体系的建设,大量中低收入群体的药品使用需求将会得到有效释放,广大的农村医药市场开始启动,也将进一步扩大包括制药市场在内的整个中国医疗保健市场的规模。这为科技创新能力强、产品质量有保障的制药企业提供了快速发展的契机。
(9)人口老龄化的趋势延续
目前,我国已逐步迈入人口老龄化时期,这将对我国社会、经济等各方面产生较大的影响。特别是对医药行业而言,人口老龄化将直接刺激我国医药消费的快速增长。发达国家经验表明,老龄化人口的医药消费占整体医药消费的50%以上。我国是目前全球老年人口增长最快的国家,截至2016年底,我国65岁及以上人口数量达到1.50亿人,占总人口的10.85%,预计到2027年我国老年人总数将超过3亿。老年人口的增多,必然会带动药品、保健品消费的需求增加。
2009-2016年中国65岁及以上人口数量及占总人口比例情况如下:
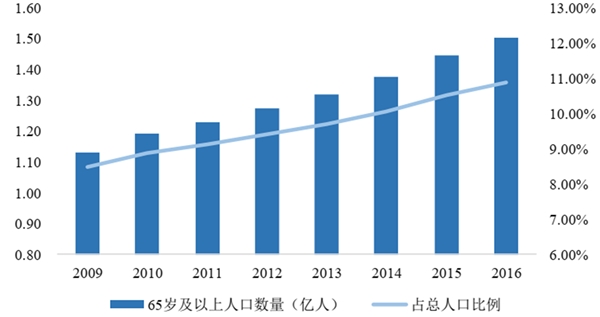
资料来源:资料公开整理
2、影响行业发展的不利因素:
(1)影响行业发展的结构性问题日益突出、研发创新相对薄弱
目前我国医药生产企业数量众多,但具有较强自主创新能力、形成规模效应的大型企业较少,大部分制药企业仍然以低端的仿制药为主,缺乏有针对性的创新,逐渐难以适应国内居民的需求。
中国医药生产企业创新能力不足已严重地制约了中国医药产业的快速发展。
虽然通过全面实施GMP和GSP认证,医药行业淘汰了一批落后企业,但总体而言,我国制药企业小、多、散的问题并未根本解决,真正具有国际竞争力和较强创新能力的大型企业很少,行业集中度偏低。
(2)药品价格受宏观调控及医保控费的影响呈下降趋势
1997年以来,为规范市场价格秩序、降低虚高的药品价格,国家发改委多次降低政府定价药品的零售价格。近年,随着《关于调整部分抗微生物类和循环系统类药品最高零售价格的通知》、《关于印发推进药品价格改革意见的通知》等一系列药品价格调控政策的出台,药品市场整体价格水平呈下降趋势,影响了医药生产企业的盈利能力。
2015年10月27日,国家卫计委、国家发改委、财政部、人社部、国家中医药管理局联合下发《关于控制公立医院医疗费用不合理增长的若干意见》,要求降低药品耗材虚高价格以及费用占比,推进医保支付方式改革,医疗费用不合理增长的势头得到初步遏制;到2017年底,公立医院医疗费用控制监测和考核机制逐步建立健全,个人支出占比逐步降低,医保控费模式将可能进一步影响药品价格的稳定。